











前 言
本标准代替GB4789.3―2010《食品安全国家标准 食品微生物学检验 大肠菌群计数》、GB/T4789.32―2002《食品卫生微生物学检验 大肠菌群的快速立博球探论坛》和SN/T0169―2010《进出口食品中大肠菌群、粪大肠菌群和大肠杆菌立博球探论坛方法》大肠菌群计数部分。
本标准与GB4789.3―2010相比,主要变化如下:
―――增加了检验原理;
―――修改了适用范围;
―――修改了典型菌落的形态描述;
―――修改了第二法平板菌落数的选择;
―――修改了第二法证实试验;
―――修改了第二法平板计数的报告。
1 范围
本标准规定了食品中大肠菌群(Coliforms)计数的方法。
本标准第一法适用于大肠菌群含量较低的食品中大肠菌群的计数;第二法适用于大肠菌群含量较高的食品中大肠菌群的计数。
2 术语和定义
2.1
大肠菌群 Coliforms
在一定培养条件下能发酵乳糖、产酸产气的需氧和兼性厌氧革兰氏阴性无芽胞杆菌。
2.2
最可能数 Mostprobablenumber;MPN
基于泊松分布的一种间接计数方法。
3 检验原理
3.1 MPN 法
MPN法是统计学和微生物学结合的一种定量立博球探论坛法。待测样品经立博国际官网稀释并培养后,根据其未生长的最低稀释度与生长的最高稀释度,应用统计学概率论推算出待测样品中大肠菌群的最大可能数。
3.2 平板计数法
大肠菌群在固体培养基中发酵乳糖产酸,在指示剂的作用下形成可计数的红色或紫色,带有或不带有沉淀环的菌落。
4 设备和材料
除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:
4.1 恒温培养箱:36℃ ±1℃。
4.2 冰箱:2℃~5℃。
4.3 恒温水浴箱:46℃±1℃。
4.4 天平:感量0.1g。
4.5 均质器。
4.6 振荡器。
4.7 无菌吸管:1mL(具0.01mL 刻度)、10mL(具0.1mL 刻度)或微量移液器及吸头。
4.8 无菌锥形瓶:容量500mL。
4.9 无菌培养皿:直径90mm。
GB4789.3―2016
4.10 pH 计或pH 比色管或精密pH 试纸。
4.11 菌落计数器。
5 培养基和试剂
5.1 月桂基硫酸盐胰蛋白胨(laurylsulfatetryptose,LST)肉汤:见A.1。
5.2 煌绿乳糖胆盐(brilliantgreenlactosebile,BGLB)肉汤:见A.2。
5.3 结晶紫中性红胆盐琼脂(violetredbileagar,VRBA):见A.3。
5.4 无菌磷酸盐缓冲液:见A.4。
5.5 无菌生理盐水:见A.5。
5.6 1mol/LNaOH 溶液:见A.6。
5.7 1mol/LHCl溶液:见A.7。
第一法 大肠菌群MPN 计数法
6 检验程序
大肠菌群MPN 计数的检验程序见图1。

图1 大肠菌群MPN 计数法检验程序
7 操作步骤
7.1 样品的稀释
7.1.1 固体和半固体样品:称取25g样品,放入盛有225mL磷酸盐缓冲液或生理盐水的无菌均质杯内8000r/min~10000r/min均质1min~2min,或放入盛有225mL磷酸盐缓冲液或生理盐水的无菌均质袋中,用拍击式均质器拍打1min~2min,制成1∶10的样品匀液。
7.1.2 液体样品:以无菌吸管吸取25mL样品置盛有225mL磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)或其他无菌容器中充分振摇或置于机械振荡器中振摇,充分混匀,制成1∶10的样品匀液。
7.1.3 样品匀液的pH 应在6.5~7.5之间,必要时分别用1mol/LNaOH 或1mol/LHCl调节。
7.1.4 用1mL 无菌吸管或微量移液器吸取1∶10样品匀液1mL,沿管壁缓缓注入9mL磷酸盐缓冲液或生理盐水的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用1支1mL无菌吸管反复吹打,使其混合均匀,制成1∶100的样品匀液。
7.1.5 根据对样品污染状况的估计,按上述操作,依次制成十倍递增立博国际官网稀释样品匀液。每递增稀释1次,换用1支1mL无菌吸管或吸头。从制备样品匀液至样品接种完毕,全过程不得超过15min。
7.2 初发酵试验
每个样品,选择3个适宜的连续稀释度的样品匀液(液体样品可以选择原液),每个稀释度接种3管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管接种1mL(如接种量超过1mL,则用双料LST肉汤),36℃±1℃ 培养24h±2h,观察倒管内是否有气泡产生,24h±2h产气者进行复发酵试验(证实试验),如未产气则继续培养至48h±2h,产气者进行复发酵试验。未产气者为大肠菌群阴性。
7.3 复发酵试验(证实试验)
用接种环从产气的LST肉汤管中分别取培养物1 环,移种于煌绿乳糖胆盐肉汤(BGLB)管中,36℃±1℃培养48h±2h,观察产气情况。产气者,计为大肠菌群阳性管。
7.4 大肠菌群最可能数(MPN)的报告
按7.3确证的大肠菌群BGLB阳性管数,检索MPN 表(见附录B),报告每g(mL)样品中大肠菌群的MPN 值。
第二法 大肠菌群平板计数法
8 检验程序
大肠菌群平板计数法的检验程序见图2。
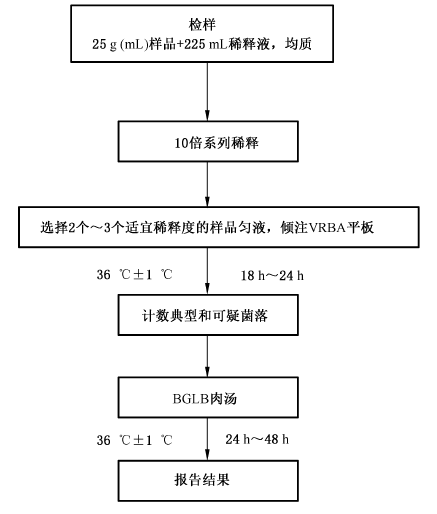
图2 大肠菌群平板计数法检验程序
9 操作步骤
9.1 样品的稀释
按7.1进行。
9.2 平板计数
9.2.1 选取2个~3个适宜的连续稀释度,每个稀释度接种2个无菌平皿,每皿1mL。同时取1mL生理盐水加入无菌平皿作空白对照。
9.2.2 及时将15mL~20mL融化并恒温至46℃的结晶紫中性红胆盐琼脂(VRBA)约倾注于每个平皿中。小心旋转平皿,将培养基与样液充分混匀,待琼脂凝固后,再加3mL~4mLVRBA 覆盖平板表层。翻转平板,置于36℃±1℃培养18h~24h。
9.3 平板菌落数的选择
选取菌落数在15CFU~150CFU 之间的平板,分别计数平板上出现的典型和可疑大肠菌群菌落(如菌落直径较典型菌落小)。典型菌落为紫红色,菌落周围有红色的胆盐沉淀环,菌落直径为0.5mm或更大,最低稀释度平板低于15CFU 的记录具体菌落数。
9.4 证实试验
从VRBA 平板上挑取10个不同类型的典型和可疑菌落,少于10个菌落的挑取全部典型和可疑菌落。分别移种于BGLB肉汤管内,36℃±1℃培养24h~48h,观察产气情况。凡BGLB肉汤管产气,即可报告为大肠菌群阳性。
9.5 大肠菌群平板计数的报告
经最后证实为大肠菌群阳性的试管比例乘以9.3中计数的平板菌落数,再乘以稀释倍数,即为每g(mL)样品中大肠菌群数。例:10-4样品稀释液1mL,在VRBA 平板上有100个典型和可疑菌落,挑取其中10个接种BGLB肉汤管,证实有6个阳性管,则该样品的大肠菌群数为:100×6/10×104/g(mL)=6.0×105CFU/g(mL)。若所有稀释度(包括液体样品原液)平板均无菌落生长,则以小于1乘以最低稀释倍数计算。
附 录 A
培养基和试剂
A.1 月桂基硫酸盐胰蛋白胨(LST)肉汤
A.1.1 成分
胰蛋白胨或胰酪胨20.0g
氯化钠5.0g
乳糖5.0g
磷酸氢二钾(K2HPO4) 2.75g
磷酸二氢钾(KH2PO4) 2.75g
月桂基硫酸钠0.1g
蒸馏水1000mL
A.1.2 制法
将上述成分溶解于蒸馏水中,调节pH 至6.8±0.2。分装到有玻璃小倒管的试管中,每管10mL。
121℃高压灭菌15min。
A.2 煌绿乳糖胆盐(BGLB)肉汤
A.2.1 成分
蛋白胨10.0g
乳糖10.0g
牛胆粉(oxgall或oxbile)溶液200mL
0.1%煌绿水溶液13.3mL
蒸馏水800mL
A.2.2 制法
将蛋白胨、乳糖溶于约500mL 蒸馏水中,加入牛胆粉溶液200mL(将20.0g脱水牛胆粉溶于200mL 蒸馏水中,调节pH 至7.0~7.5),用蒸馏水稀释到975mL,调节pH 至7.2±0.1,再加入0.1%煌绿水溶液13.3mL,用蒸馏水补足到1000mL,用棉花过滤后,分装到有玻璃小倒管的试管中,每管10mL。121℃高压灭菌15min。
A.3 结晶紫中性红胆盐琼脂(VRBA)
A.3.1 成分
蛋白胨7.0g
酵母膏3.0g
乳糖10.0g
氯化钠5.0g
胆盐或3号胆盐1.5g
中性红0.03g
结晶紫0.002g
琼脂15g~18g
蒸馏水1000mL
A.3.2 制法
将上述成分溶于蒸馏水中,静置几分钟,充分搅拌,调节pH 至7.4±0.1。煮沸2min,将培养基融化并恒温至45℃~50℃倾注平板。使用前临时制备,不得超过3h。
A.4 磷酸盐缓冲液
A.4.1 成分
磷酸二氢钾(KH2PO4) 34.0g
蒸馏水500mL
A.4.2 制法
贮存液:称取34.0g的磷酸二氢钾溶于500mL蒸馏水中,用大约175mL的1mol/L氢氧化钠溶液调节pH 至7.2±0.2,用蒸馏水稀释至1000mL后贮存于冰箱。稀释液:取贮存液1.25mL,用蒸馏水稀释至1000mL,分装于适宜容器中,121℃高压灭菌15min。
A.5 无菌生理盐水
A.5.1 成分
氯化钠8.5g
蒸馏水1000mL
A.5.2 制法
称取8.5g氯化钠溶于1000mL蒸馏水中,121℃高压灭菌15min。
A.6 1mol/LNaOH 溶液
A.6.1 成分
NaOH 40.0g
蒸馏水1000mL
A.6.2 制法
称取40g氢氧化钠溶于1000mL无菌蒸馏水中。
A.7 1mol/LHCl溶液
A.7.1 成分
HCl 90mL
蒸馏水1000mL
A.7.2 制法
移取浓盐酸90mL,用无菌蒸馏水稀释至1000mL。
附 录 B
大肠菌群最可能数(MPN)检索表
B.1 大肠菌群最可能数(MPN)检索表
每g(mL)检样中大肠菌群最可能数(MPN)的检索见表B.1。
表B.1 大肠菌群最可能数(MPN)检索表


传真:0532-81935080 66087775
邮箱:qdhbywg@vip.126.com
QQ:4000532596